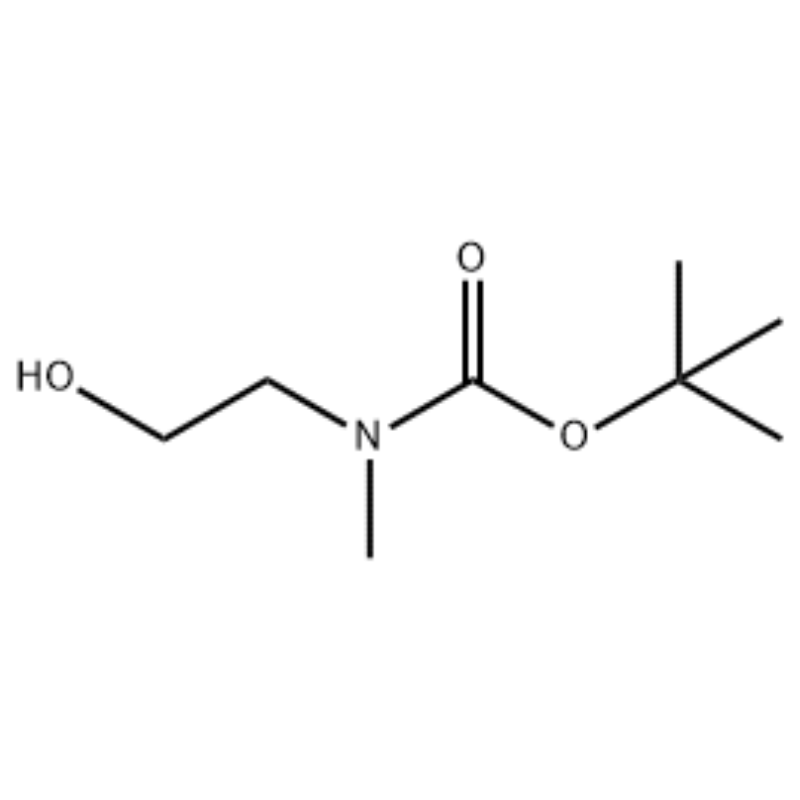
CH2Cl2 (20 ml) मध्ये 2-(methylamino) इथेनॉल (500 mg, 0.53 ml, 6.66 mmol) च्या द्रावणात Boc2O (1.48 g, 6.79 mmol) जोडले गेले, त्यानंतर खोलीच्या तापमानाला 1 तास ढवळत राहा.ब्राइन आणि CH2Cl2 सह प्रतिक्रिया द्रावण काढले गेले.अशा प्रकारे प्राप्त झालेला सेंद्रिय थर MgSO4 वर वाळवला गेला आणि फिल्टर केला गेला.नंतर, ऑब्जेक्ट कंपाऊंड (रंगहीन तेल, परिमाणवाचक) मिळविण्यासाठी फिल्टर व्हॅक्यूओमध्ये केंद्रित केले गेले;1H NMR (200 MHz, CDCl3) डेल्टा 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);मास स्पेक्ट्रम m/e (सापेक्ष तीव्रता) 144 (20) 102 (24) 57 (70) 44 (100).
उदाहरण 38;N1-(3-Fluoro-4-(2-(1-(2-(methylamino)ethyl)-1H-imidazol-4-yl)thieno[3,2-b]pyridin-7-yloxy)phenyl)-N3 -(2-मेथोक्सीफेनिल)मॅलोनामाइड (96);पायरी 1: tert-Butyl 2-hydroxyethyl(methyl)carbamate (97) (J. Med. Chem., 1999, 42, 11, 2008) मध्ये 2-(methylamino) इथेनॉल (5.0 g, 67 mmol) च्या द्रावणासाठी RT वर THF (50 ml) Boc2O (15.7 g, 72 mmol) जोडले गेले आणि प्रतिक्रिया मिश्रण RT वर 4 तास ढवळले.प्रतिक्रिया मिश्रण कोरडेपणावर केंद्रित केले गेले आणि शीर्षक कंपाऊंड 97 थेट पुढील चरणात कोणत्याही अतिरिक्त शुद्धीकरणाशिवाय वापरले गेले (11.74 ग्रॅम, 100% उत्पन्न).MS (m/z): 176.2 (M+H).
l-2-[4-Bromo-2-(4-oxo-2-ftiotaioxo1hiazolidin-5-ylidenemefliyl)phenoxy]efliyl-3-efliyl-l- methylurea(Compoiotamd 161)चरण 1 : t-butyl2- चे संश्लेषण hydroxythylmethylcarbamate;CH2Cl2 (20 ml) मध्ये 2-(methylamino) इथेनॉल (500 mg, 0.53 ml, 6.66 mmol) च्या द्रावणात BoC2O (1.48 g,6.79 mmol) जोडले गेले, त्यानंतर खोलीच्या तापमानाला 1 तास ढवळत राहा.ब्राइन आणि CH2Cl2 सह प्रतिक्रिया द्रावण काढले गेले.अशा प्रकारे प्राप्त झालेला सेंद्रिय थर MgSO4 वर वाळवला गेला आणि फिल्टर केला गेला.नंतर, ऑब्जेक्ट कंपाऊंड (रंगहीन तेल, परिमाणवाचक) मिळविण्यासाठी फिल्टर व्हॅक्यूओमध्ये केंद्रित केले गेले; 1HNMR (200 MHz, CDCl3) डेल्टा 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);मास स्पेक्ट्रम m/e (सापेक्ष तीव्रता) 144 (20) 102 (24) 57 (70) 44 (100).
2-(मेथिलामिनो) इथेनॉल (90.1 g, 1.2 mol) 1.2 L मिथिलीन क्लोराईडमध्ये विरघळले गेले आणि BoC2O (218 g, 1 mol) 00C वर ढवळत असताना त्यात हळूहळू जोडले गेले, त्यानंतर खोलीच्या तपमानावर 3 तास.संतृप्त अमोनियम क्लोराईडच्या जलीय द्रावणाच्या 700 एमएल आणि 300 एमएल पाण्याने प्रतिक्रियांचे मिश्रण क्रमाने धुतले गेले.धुतलेले मिश्रण निर्जल सोडियम सल्फेट वापरून निर्जलीकरण केले गेले आणि कमी दाबाने केंद्रित केले गेले, मिश्रण (a) (175 g, 1 mol, 100%) तेल म्हणून रंग नसलेले प्राप्त करण्यासाठी. TLC : Rf = 0.5 (50% EtOAc in Hex) Ce-Mo stain1H NMR (600MHz, CDCl3) डेल्टा 1.47 (s, 9H), 2.88 (br s, IH), 3.41 (br s, 2H), 3.76 (br s, 2H) सह व्हिज्युअलाइज्ड.
2-(मेथिलामिनो) इथेनॉलचे 90.1 ग्रॅम (1.2 मोल) 1.2 एल मिथिलीन क्लोराईडमध्ये विरघळले गेले, 218 ग्रॅम (1 मोल) Boc2O त्यात हळूहळू जोडले गेले, परिणामी द्रावण 0C वर ढवळले आणि परिणामी द्रावण ढवळले. खोलीचे तापमान 3 तास.अभिक्रिया मिश्रण अनुक्रमे 700 मिली जलीय संतृप्त अमोनियम क्लोराईड द्रावण आणि 300 मिली पाण्याने धुतले जाते, निर्जल सोडियम सल्फेटचा वापर करून निर्जलीकरण केले जाते आणि नंतर कमी दाबाने 175 ग्रॅम (1 mol) ॲक्रोमिक ऑइल कंपाऊंडद्वारे संरक्षित केले जाते. Boc गट (उत्पन्न: 100%).[0140] 1H NMR (600MHz, CDCl3) डेल्टा 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (br s, 2H) , J = 15.0 Hz, 3H), 1.46 (d, J = 16.2 Hz, 9H) [0141] 90 g (0.514 mol) प्राप्त कंपाऊंड 1.5 L tetrahydrofuran मध्ये विरघळले, 88.0 g (539 N- mol) त्यात हायड्रॉक्सीफथालिमाइड आणि 141 ग्रॅम (0.539 mol) ट्रायफेनिलफॉस्फिन जोडले गेले, 0C वर परिणामी द्रावण ढवळत असताना त्यात 106 mL (0.539 mol) diisopropyl azodicarboxylate हळूहळू जोडले गेले आणि परिणामी द्रावण ढवळत असताना तापमान 3 तास वाढवले गेले. खोलीच्या तापमानाला.कमी दाबाखाली प्रतिक्रिया मिश्रणाच्या एकाग्रतेनंतर, त्यात 600 एमएल आयसोप्रोपायलेथर जोडले गेले, परिणामी द्रावण 0C वर 1 तास ढवळले आणि पांढरा घन-प्रकार ट्रायफेनिलफॉस्फिन ऑक्साईड फिल्टर केला गेला.घन पदार्थ 200 मिली आयसोप्रोपायलेथरने 0C पर्यंत थंड करून प्रथम गाळण्याने धुतले गेले आणि परिणामी गाळण कमी दाबाने केंद्रित करून 198 ग्रॅम कंपाऊंड XX आणि डायसोप्रोपाइल हायड्रॅझोडिकार्बोक्झिलेटचे मिश्रण 10% ते 10% या प्रमाणात मिळते. (उत्पन्न: 120%).[0142] 1H NMR (600MHz, CDCl3) डेल्टा 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (br s, 2H) , J = 15.0 Hz, 3H), 1.46 (d, J= 16.2 Hz, 9H)
 बिल्डिंग 12, क्र.309, साउथ 2रा रोड, इकॉनॉमिक डेव्हलपमेंट झोन, लाँगक्वानी जिल्हा, चेंगडू, सिचुआन, चीन.
बिल्डिंग 12, क्र.309, साउथ 2रा रोड, इकॉनॉमिक डेव्हलपमेंट झोन, लाँगक्वानी जिल्हा, चेंगडू, सिचुआन, चीन. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +८६ (०२८) ८४८४१९६९
+८६ (०२८) ८४८४१९६९ +८६ १३५ ५८८५ ५४०४
+८६ १३५ ५८८५ ५४०४



















.png)


